시애틀 기반 COVID-19 백신 두 종류, 주요 규제 승인 획득
1 min read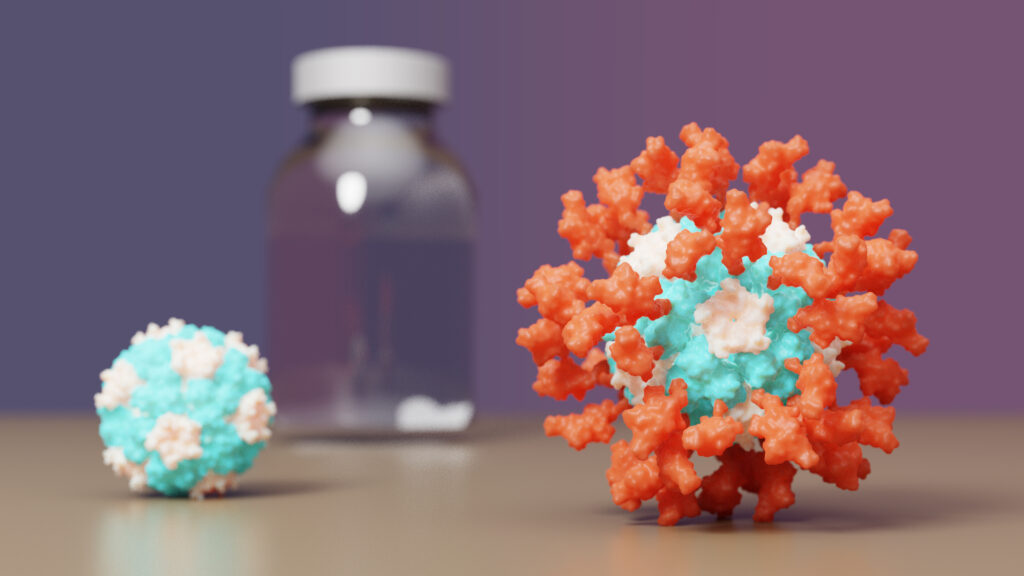
이미지 출처:https://www.geekwire.com/2022/covid-19-shots-with-seattle-origins-reach-regulatory-milestones-in-south-korea-india/
수요일, 시애틀에 뿌리를 둔 두 가지 COVID-19 백신이 주요 규제 마일스톤을 통과했다. 워싱턴 대학교가 개발한 백신이 한국에서 승인되었고, 인도 규제 당국이 시애틀 스타트업 HDT Bio와 관련된 또 다른 백신에 대해 긴급 사용 승인을 부여했다.
두 백신 모두 냉장 온도에서 안정적이며, COVID-19 백신 접종이 부족한 지역을 포함하여 전 세계 배급을 염두에 두고 개발되었다.
워싱턴 대학교의 단백질 기반 백신은 생화학 연구원인 David Veesler와 UW 단백질 설계 연구소의 Neil King의 연구실에서 시작되었다. King은 GeekWire와의 인터뷰에서 이 백신이 “의학에서 컴퓨터 설계 단백질의 출현을 알리는 것”이라고 말했다.
이 백신은 바이러스 스파이크 단백질의 일부를 장착한 구형 입자로 되어 있으며, 개별 성분에서 스스로 조립되어 제조가 용이하다.
워싱턴 대학교의 이 백신은 한국 생명공학 기업인 SK bioscience에 라이선스가 부여되었으며, GSK의 면역 증진 기능을 가진 아즈주반트와 결합되었다. 이 백신은 SKYCovione라는 이름으로 알려져 있다.
한국 식품의약품안전처는 SKYCovione를 18세 이상의 성인에게 승인했으며, 한국 정부는 국내 사용을 위해 1천만 도스를 구매하기로 합의했다.
또한 SK bioscience는 세계 보건 기구에 대한 긴급 사용 목록 승인을 위해 다른 규제 기관에 대한 승인을 요청하고 있다.
HDT Bio에서 개발한 백신은 Moderna와 Pfizer/BioNTech의 승인된 백신과 마찬가지로 RNA 기반이다. 그러나 이 새로운 백신의 RNA는 여러 개의 복사본을 생성하도록 설계되어, 더 낮은 용량과 비용으로 강력한 백신을 제공한다.
HDT는 이 백신을 인도 푸네에 기반을 둔 Emcure의 자회사인 Gennova Biopharmaceuticals에 라이선스하였다. 현재 Emcure는 HDT의 상업 비밀을 도용하고 임상 데이터를 공유하지 않았다는 소송에 연루되어 있다.
회사는 이 백신의 3상 연구 결과를 아직 발표하지 않았다. Gennova는 현재 700만 도스를 보유하고 있으며, 배포를 위한 준비가 되어 있다.
King은 GeekWire 서밋에서의 연설에서 “이 백신은 컴퓨터 설계 기반으로 승인된 첫 번째 백신 또는 치료법이다”라고 말했다. 그는 “이는 중대한 순간”이라고 덧붙였다.
SK bioscience의 데이터에 따르면, SKYCovione는 강력한 면역 반응을 유도하는 것으로 나타났다.
SK bioscience는 SKYCovione를 18세 이상의 성인 4,037명을 대상으로 한 2회 접종 3상 임상 시험에서 테스트하였다.
이 연구에 따르면, SKYCovione는 아스트라제네카의 백신인 Vaxzevria보다 COVID-19의 원래 변종에 대한 더 강력한 면역 반응을 보였다.
SKYCovione는 바이러스에 대한 “중화” 항체가 아스트라제네카 접종자에 비해 3배 더 생성되었다.
King은 SKYCovione가 RNA 백신과 직접 테스트되지 않았지만, SK bioscience의 데이터에 기반하여 SKYCovione는 “최소한 같은 정도로 강력하다”고 추측했다.
이전의 백신들은 질병에 대한 임상 효능을 기반으로 승인되었으나, 면역 측정 방법이 보호와 어떤 상관관계를 가지는지에 대한 이해가 높아짐에 따라 이러한 방식이 더욱 일반화될 것이라고 Veesler는 이메일을 통해 말했다.
예를 들어, 최근 Fred Hutchinson Cancer Center의 연구자들이 이끄는 연구는 Novavax 백신에 대한 보호가 중화 항체와 일치한다는 것을 보여주었다.
SKYCovione의 초기 임상 시험 데이터는 현재 프리프린트 연구로 제공되고 있으며, 3상 데이터는 곧 발표될 예정이다.
SK bioscience는 현재 SKYCovione를 오미크론 및 기타 COVID-19 변종에 대해 평가하는 연구를 진행하고 있다.
이 플랫폼은 다양한 변종에 대한 백신으로 사용될 가능성이 있다고 King은 전했다.
연구팀은 다양한 변종의 단백질 조각으로 나노입자를 장착할 계획이다.
King과 그의 동료들은 백신 상용화 방안을 생각할 때 두 가지 경로를 택하였다. 하나는 SK Bioscience에 기술을 라이선스하는 것이었고, 다른 하나는 UW 백신 스타트업인 Icosavax 내에서 개발하는 것이었다.
이 전략은 필요시 신속하게 팬데믹을 도울 수 있었던 것으로 여겨져, 상황이 더 복잡해지지 않았다.
King은 이 모든 결정들이 ‘두 번의 기회를 구축하라’는 전략 내에서 이루어진 것이라 고백했다.
사실, Icosavax가 진행한 초기 임상 연구 데이터는 SKYCovione보다 면역 반응이 뛰어나지 않았다는 것을 보여주었다.
따라서 Icosavax는 제조 접근 방식이나 사용하는 아즈주반트의 차이 때문일 수 있음을 조사하고 있다.
HDT는 또한 호흡기 세포융합 바이러스에 대한 다른 백신에 대한 초기 단계의 임상 시험 데이터를 수요일에 발표하였다.
워싱턴 대학교의 백신은 이미 승인된 B형 간염 및 인유두종 바이러스 백신과 동일한 청사진을 갖고 있다.
King은 “우리의 백신이 더 전통적인 백신 방식이라고 주장할 수 있다”고 말했다.
소프트웨어는 단순히 최상의 설계를 생성하는 데 도움이 되었다는 것이다.
SKYCovione의 승인은 빠르게 성장하는 컴퓨터 단백질 설계 분야에서 향후 신약 개발에 대한 길을 열어줄 것으로 예상된다.






